
El nostre grup se centra en la interacció entre les respostes a l’estrès, la plasticitat cel·lular i el càncer. La plasticitat cel·lular es reconeix avui dia com una característica crítica de les cèl·lules canceroses que els permet transitar entre diferents estats cel·lulars i afavorir el creixement tumoral, la progressió de la malaltia després de la teràpia i la metàstasi.
Amb anterioritat, hem constatat que induir la desdiferenciació amb els anomenats factors de Yamanaka pot donar lloc al desenvolupament de diferents tumors. També hem demostrat que el dany tissular, principal impulsor del càncer, desencadena l’inici de la senescència cel·lular, que després indueix la desdiferenciació i l’adquisició de propietats de les cèl·lules mare in vivo.
Aquestes observacions tenen importants implicacions terapèutiques, atès que la quimioteràpia i la radioteràpia, pedres angulars per al tractament de la majoria dels tipus de càncer, podrien tenir l’efecte secundari d’induir la formació de cèl·lules mare a les cèl·lules canceroses no mare i, a alhora, contribuir a la recurrència del tumor i la disseminació de les cèl·lules canceroses.
El nostre principal objectiu és avançar en el coneixement dels mecanismes i impulsors implicats en aquest procés, amb la finalitat de desenvolupar nous tractaments a partir de la inhibició de la plasticitat de les cèl·lules canceroses.
Diferents troballes recents han demostrat que algunes regions genòmiques, abans considerades no codificants (inclosos els lncRNA), contenen petits marcs de lectura oberts que codifiquen microproteïnes no anotades i conservades evolutivament. Les poques que s’han identificat fins ara assumeixen funcions clau en processos cel·lulars elementals, cosa que dóna lloc a un nou nivell de complexitat amb implicacions importants, des de la recerca bàsica fins a l’àmbit clínic.
En els darrers anys, els nostres esforços s’han centrat a descobrir i descriure noves microproteïnes cancerígenes que podrien ser nous actors a la carcinogènesi. El nostre grup ha identificat cinc noves microproteïnes del càncer i hem obtingut proves convincents in vitro i in vivo que quatre actuen com a nous supressors tumorals, induint la detenció del cicle cel·lular, la diferenciació o la inhibició dels trets mesenquimals de les cèl·lules canceroses . A més, amb l’ús d’un enfocament petidòmic hem identificat un conjunt de microproteïnes segregades per tumors pancreàtics, ja siguin solubles o en exosomes. Aquestes noves microproteïnes podrien ser missatgers cel·lulars crucials per a la metàstasi del càncer de pàncrees. La identificació de microproteïnes tumorals podria ser clau per avançar en el coneixement de la fisiopatologia del càncer. A més, també podrien servir com a nous biomarcadors del càncer per a la detecció precoç de la malaltia i l’estratificació de pacients per a tractaments a mida, així com per a les dianes terapèutiques.
- Avançar en el coneixement de la interacció entre la senescència induïda per la teràpia, la plasticitat cel·lular i el càncer.
- Desxifrar els mecanismes moleculars que regeixen l’adquisició de propietats de les cèl·lules mare durant l’oncogènesi i després de la teràpia.
- Descobrir i caracteritzar noves microproteïnes implicades en la plasticitat de les cèl·lules canceroses.
- Desenvolupar noves teràpies antineoplàstiques basades en la inhibició de la plasticitat de les cèl·lules canceroses.
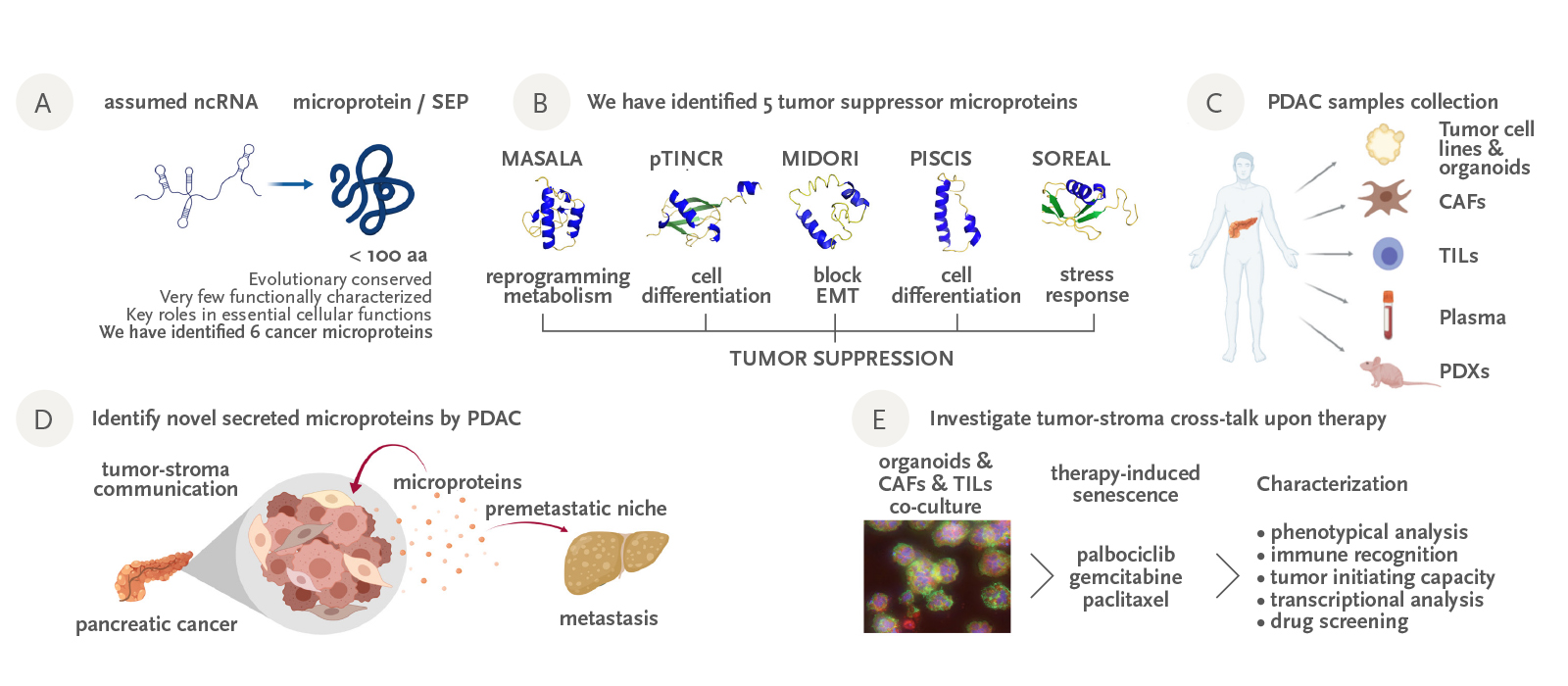
Figura: A) Descobriments recents han revelat que moltes regions genòmiques abans considerades com a no codificants en realitat codifiquen microproteïnes no anotades; algunes han demostrat ser importants per al càncer. B) El nostre grup ha identificat cinc noves microproteïnes amb activitats supressores de tumors. Les hem caracteritzat in vitro i in vivo. C) Hem generat una àmplia col·lecció de mostres de càncer de pàncrees amb pacients associats i que serà fonamental per a la nostra recerca. D) Estem investigant si les cèl·lules canceroses utilitzen microproteïnes secretades no anotades com a missatgers intercel·lulars per afavorir el creixement tumoral i la metàstasi. E) Estem establint col·lectius d’organoides-CAF-LIT per investigar l’impacte de la teràpia en la interacció entre tumor i estroma.
Cap de grup
María Abad
Assistent de recerca
Lluis Palenzuela
Estudiants de postgrau
Alba Escriche
Marion Martinez
- Marin I, Boix O, Garcia-Garijo A, Sirois I, Caballe A, Zarzuela E, Ruano I, Attolini CS, Prats N, López-Domínguez JA, Kovatcheva M, Garralda E, Muñoz J, Caron E, Abad M, Gros A, Pietrocola F, Serrano M. Cellular Senescence Is Immunogenic and Promotes Antitumor Immunity. Cancer Discov. 2023 Feb 6;13(2):410-431.
- Pujals M, Mayans C, Bellio C, Méndez O, Greco E, Fasani R, Alemany-Chavarria M, Zamora E, Padilla L, Mitjans F, Nuciforo P, Canals F, Nonell L, Abad M, Saura C, Tabernero J, Villanueva J. RAGE/SNAIL1 signaling drives epithelial-mesenchymal plasticity in metastatic triple-negative breast cancer. Oncogene. 2023 Aug;42(35):2610-2628.
- Álvarez-Sierra D, Sánchez-Gaona N, Cruz Cobo M, Escriche A, Abad M, Gómez-Brey A, Bello I, Caubet E, González Ó, Zafón C, Iglesias C, Moreno P, Petit A, Fernández-Sanmartín MA, Martínez-Gallo M, Pujol-Borrell R. Thyroid cells from normal and autoimmune thyroid glands suppress T lymphocytes proliferation upon contact revealing a new regulatory inhibitory type of interaction independent of PD1/PDL1. J Autoimmun. 2023 Apr;136:103013.
- Boix O, Martinez M, Vidal S, Giménez-Alejandre M, Palenzuela L, Lorenzo-Sanz L, Quevedo L, Moscoso O, Ruiz-Orera J, Ximénez-Embún P, Ciriaco N, Nuciforo P, Stephan-Otto Attolini C, Albà MM, Muñoz J, Tian TV, Varela I, Vivancos A, Ramón Y Cajal S, Muñoz P, Rivas C, Abad M. pTINCR microprotein promotes epithelial differentiation and suppresses tumor growth through CDC42 SUMOylation and activation. Nat Commun. 2022 Nov 11;13(1):6840.
- Marin I, Boix O, Garcia-Garijo A, Sirois I, Caballe A, Zarzuela E, Ruano I, Stephan-Otto Attolini C, Prats N, Lopez-Dominguez JA, Kovatcheva M, Garralda E, Munoz J, Caron E, Abad M, Gros A, Pietrocola F, Serrano M. Cellular senescence is immunogenic and promotes anti-tumor immunity. Cancer Discov. Epub 2022 Oct 27.
- Senís E, Esgleas M, Najas S, Jiménez-Sábado V, Bertani C, Giménez-Alejandre M, Escriche A, Ruiz-Orera J, Hergueta-Redondo M, Jiménez M, Giralt A, Nuciforo P, Albà MM, Peinado H, Del Toro D, Hove-Madsen L, Götz M, Abad M. TUNAR lncRNA Encodes a Microprotein that Regulates Neural Differentiation and Neurite Formation by Modulating Calcium Dynamics. Front Cell Dev Biol. 2021 Dec 31;9:747667.
- Senís E, Mosteiro L, Grimm D, Abad M. A Versatile In Vivo System to Study Myc in Cell Reprogramming. Methods Mol Biol. 2021;2318:267-279.
- Senís E, Mosteiro L, Grimm D, Abad M. Methods Mol Biol. 2021;2318:267-279. doi: 10.1007/978-1-0716-1476-1_14.
- Salazar-Roa M, Trakala M, Alvarez-Fernandez M, Valdes-Mora F, Munoz J, Zapatero-Solana E, Grana O, Peters T,Abad M, Bueno M, Gomez de Cedron M, Fernandez-Piqueras J, De Martino A, Serrano M, Wang D, Clark S, Ortega S and Malumbres M. Transient exposure to miR-203 enhances the differentiation capacity of established pluripotent stem cells. In press. Embo Journal. DOI:10.15252/embj.2019104324
- Merino I, Greco E,Abad M(2020). The microproteome of cancer: from invisibility to relevance.Experimental Cell Research. 2020;392(1):111997. doi:10.1016/j.yexcr.2020.111997
- Senís E, Mosteiro L, Wilkening S, Wiedtke E, Nowrouzi A, Afzal S, Fronza R, Landerer H,Abad M, Niopek D, Schmidt M, Serrano M, Grimm D.AAVvector-mediated in vivo reprogramming into pluripotency.Nat Commun. 2018 Jul 9;9(1):2651. doi: 10.1038/s41467-018-05059-x.
- Abad M, Hashimoto H, Zhou H, Morales MG, Chen B, Bassel-Duby R, Olson EN.Notch Inhibition Enhances Cardiac Reprogramming by Increasing MEF2C Transcriptional Activity. Stem Cell Reports. 2017 Mar 14;8(3):548-560.
- Marión RM, López de Silanes I, Mosteiro L, Gamache B, Abad M, Guerra C, Megías D, Serrano M, Blasco MA.Common Telomere Changes during In Vivo Reprogramming and Early Stages of Tumorigenesis. Stem Cell Reports. 2017 Feb 14;8(2):460-475.
- Gómez-Cabello D, Checa-Rodríguez C, Abad M, Serrano M, Huertas P.CtIP-Specific Roles during Cell Reprogramming Have Long-Term Consequences in the Survival and Fitness of Induced Pluripotent Stem Cells. Stem Cell Reports. 2017 Feb 14;8(2):432-445.
- Mosteiro L, Pantoja C, Alcázar N, Marión RM, Chondronasiou D, Rovira M, Fernández-Marcos PJ, Muñoz M, Blanco-Aparicio C, Pastor J, Gómez-López G, de Martino A, Blasco MA, Abad M and Serrano M. Tissue damage and senescence provide critical signals for cellular reprogramming in vivo. Science. 2016 Nov 25;354(6315). pii: aaf4445.
- Adrados I., Larrasa J., Galarreta A., López-Antona I., Menendez C., Abad M., Gil J., Moreno-Bueno G. And Palmero I. The homeoprotein SIX1 controls cellular senescence through the regulation of p16INK4A and differentiation-related genes. Oncogene. 2016 Jul 7;35(27):3485-94
- Vilas JM, Ferreirós A, Carneiro C, Morey L, Da Silva-Álvarez S, Fernandes T, Abad M, Di Croce L, García-Caballero T, Serrano M, Rivas C, Vidal A, Collado M. Transcriptional regulation of Sox2 by the retinoblastoma family of pocket proteins. Oncotarget. 2015 Feb 20;6(5):2992-3002.
- Palla A.R., Piazzolla D., Abad M., Li H., Dominguez O., Schönthaler H.B., Wagner E.F. and Serrano M.Reprogramming activity of NANOGP8, a NANOG family member widely expressed in cancer. Oncogene.2014 May 8;33(19):2513-9
- Abad M, Mosteiro L, Pantoja C, Cañamero M, Rayon T, Ors I, Graña O, Megías D, Domínguez O, Martínez D, Manzanares M, Ortega S, Serrano M.Reprogramming in vivo produces teratomas and iPS cells with totipotency features. Nature. 2013 Oct 17;502(7471):340-5.
- Abad M, Moreno A, Palacios A, Narita M, Blanco F, Moreno-Bueno G, Narita M and Palmero I.The tumor suppressor ING1 contributes to epigenetic control of cellular senescence. Aging Cell. 2011 Feb; 10:158-71.
- Menéndez C, Abad M, Gómez-Cabello D, Moreno A and Palmero I. ING proteins in cellular senescence. Curr Drug Targets. 2009 May;10:406-1.
- Abad M, Menéndez C, Fuchtabuer A, Serrano M, Fuchtbauer E-M and Palmero I.Ing1 mediates p53 accumulation and chromatin modification in response to oncogenic stress.J Biol Chem. 2007 Oct 19;282:31060-7
- Goeman F.,Thormeyer D., Abad M., Serrano M., Schmidt O., Palmero I. and Baniahmad A. Growth inibition by the tumor suppressor p33ING1 in immortalized and primary cells: Involvement of two silencing domains and effect of Ras.Mol Cell Biol. 2005 Jan;25:422-31.
- Tumoral senescence induced by anti-cancer therapies constitutes a novel prognostic biomarker and a therapeutic target.
Reference: PRYCO211023SERR.
Spanish Association Against Cancer – AECC.
Award Period: 9/2021-8/2026
Co-PI: María Abad. - Defining the Role of Exosome-Secreted Micropeptides in Pancreatic Cancer. number: HR18-00256.
Health Research Grant-La Caixa Foundation.
Award Period: 9/2019-8/2021.
PI: Maria Abad. - Identificación y Análisis del Microproteoma del Cáncer de Páncreas: Los Micropéptidos como Nuevas Dianas Terapéuticas y Biomarcadores Tumorales Fundación. XVI Convocatoria de Ayudas a la Investigación en Salud.
Fundación Mutua Madrileña.
01/09/2019-30/08/2022.
PI: Maria Abad. - Mining the Microproteome for New Molecular Targets in Cancer.
number: RTI2018-102046-B-I00.Spanish Ministry of Economy and Competitiveness.
1/2019-12/2021.
PI: Maria Abad.













