
- Els resultats de l’assaig clínic fase I, publicats a la revista de l’European Society of Medical Oncology (ESMO), indiquen que l’anticòs MSC-1 desenvolupat pel grup del Dr. Seoane a VHIO és segur i ben tolerat en pacients amb tumors sòlids avançats. La missió del nou fàrmac és bloquejar la proteïna LIF, que es troba alterada en diversos tipus de càncer, que promou la proliferació de cèl·lules mare tumorals i desactiva la resposta del sistema immunitari contra el tumor.
- En aquest assaig hi han participat 41 pacients a l’Hospital Universitari Vall d’Hebron, al Memorial Sloan Kettering Cancer Center (Nova York) i a l’Hospital Princess Margaret (Toronto).
- Paral·lelament als resultats de l’assaig, els investigadors liderats pel Dr. Joan Seoane han publicat un estudi a la revista Clinical Cancer Research on descriuen els mecanismes moleculars implicats en l’efecte antitumoral d’MSC-1.
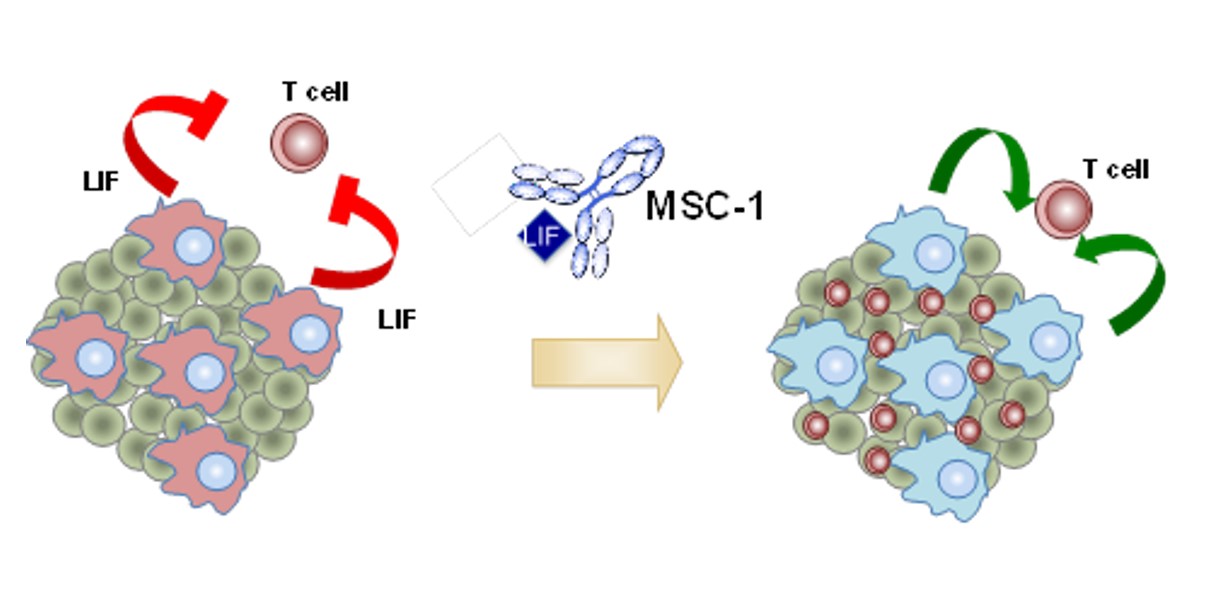
- Tant els resultats de l’assaig clínic com els models preclínics mostren com el fàrmac MSC-1 actua mitjançant el microambient tumoral. En concret, MSC-1 converteix els macròfags immunosupressors en immunoestimuladors i indueix la infiltració de cèl·lules immunitàries antitumorals (cèl·lules T) al tumor, que actuen contra les cèl·lules tumorals.
- Aquests resultats són la base de l’assaig clínic fase II ja obert que es du a terme combinant MSC-1 amb anti-PD-L1. Vall d’Hebron és un dels centres participants en l’assaig amb la Dra. Teresa Macarulla, cap del Grup de Tumors Gastrointestinals i Endocrins del VHIO i metgessa oncòloga de l’Hospital Universitari Vall d’Hebron, com a investigadora principal.
El fàrmac MSC-1 dissenyat pel grup liderat pel Dr. Joan Seoane al Vall d’Hebron Institut d’Oncologia (VHIO), que forma part del Campus Vall d’Hebron, ha demostrat que és un fàrmac segur i ben tolerat en pacients amb tumors sòlids avançats.
Són els resultats que publica la revista ESMO Open del primer assaig clínic en fase I d’MSC-1 que s’ha dut a terme en 41 pacients amb càncer de pàncrees, còlon, cap i coll, ovari o pròstata, tots en estat avançat, i que havien estat tractats prèviament amb diversos tractaments oncològics. L’objectiu de l’assaig era determinar la seguretat i la tolerabilitat, la dosi recomanada per a la fase II de l’assaig, la farmacodinàmica i la farmacocinètica de l’anticòs monoclonal MSC-1. Els pacients tractats amb MSC-1 no van presentar toxicitat a cap de les dosis subministrades, ni efectes adversos greus relacionats amb el tractament. A més, es van poder estudiar biòpsies dels pacients per entendre el mecanisme d’acció del fàrmac.
Els resultats avalen LIF com una diana terapèutica en el context del càncer
«La missió d’MSC-1 és bloquejar la proteïna LIF», explica el Dr. Joan Seoane, professor investigador d’ICREA i codirector del Programa de Recerca Preclínica i Translacional del VHIO. «Aquesta proteïna està involucrada en diversos processos fisiològics i patològics. Participa per dues vies en el desenvolupament embrionari: d’una banda, protegeix l’embrió del sistema immunitari de la mare promovent un ambient immunosupressor, i de l’altra promou la proliferació de cèl·lules mare durant el desenvolupament de l’embrió».
«En alguns tipus de càncer els nivells de LIF estan alterats, de manera que el tumor s’apropia de les funcions d’aquesta proteïna per desactivar el sistema immunitari contra les cèl·lules tumorals i incrementar el nombre de cèl·lules mare tumorals, impulsant el creixement i la progressió del tumor», afegeix l’investigador.
L’anticòs MSC-1 bloqueja la senyalització de la proteïna LIF de manera que, d’una banda, activa la resposta immunitària antitumoral i, de l’altra, inhibeix les cèl·lules mare tumorals en pacients amb tumors sòlids avançats.
«Els resultats d’aquest assaig avalen la nostra hipòtesi que LIF podria ser una diana terapèutica per tractar pacients amb tumors sòlids avançats. De fet, ja hem iniciat un assaig clínic fase II d’MSC-1 ‒ara AZD0171‒ en combinació amb l’agent immunoterapèutic anti-PD-L1 en pacients amb càncer de pàncrees avançat. Els resultats d’aquest assaig fase II haurien de determinar l’eficàcia antitumoral del fàrmac», explica el Dr. Joan Seoane.
Primeres evidències de reactivació del sistema immunitari pel bloqueig de LIF en humans
«Al primer assaig d’MSC-1 en humans s’han observat les primeres evidències d’activitat immunoactivadora a través de l’estudi de les biòpsies dutes a terme. La presència de biomarcadors d’activació immunològica a l’ambient tumoral suporta la hipòtesi terapèutica d’MSC-1», afirma el Dr. Seoane.
Tot i així, l’objectiu d’un assaig clínic fase I no és l’estudi de l’eficàcia del fàrmac. En els pacients tractats durant l’assaig clínic es va observar que en nou pacients (23,7%) el tumor va parar de créixer. En el cas d’un pacient amb càncer de pàncrees avançat i tractat prèviament amb qutre fàrmacs diferents, es va observar una reducció del tumor del 40% en una de les lesions. Els resultats van indicar que el tractament en combinació amb un altre fàrmac podria ser efectiu.
«Estudiar com responen al tractament els pacients amb determinades expressions anormals de LIF ens fa avançar cap a una medicina precisió que ens permeti prendre les decisions terapèutiques òptimes per a cada pacient i proposar la combinació terapèutica adequada», apunta el Dr. Joan Seoane.
Mecanismes moleculars de LIF en la modulació de la resposta del sistema immunitari
En aquest sentit, i paral·lelament a la publicació dels resultats de l’assaig, el grup liderat pel Dr. Seoane ha publicat un nou estudi a la revista Clinical Cancer Research que descriu els mecanismes moleculars del fàrmac MSC-1.
«Cada vegada coneixem més bé com el microambient tumoral format per diferents tipus de cèl·lules que acompanyen el tumor pot influir en la progressió del tumor», explica el Dr. Seoane. «En aquest microambient trobem macròfags, cèl·lules que en condicions normals actuen com a primera línia de defensa de l’organisme. No obstant això, en el microambient tumoral els macròfags associats al tumor (TAM) poden ser immunosupressors i són capaços de desactivar la resposta del sistema immunitari contra les cèl·lules tumorals, impulsant-ne la progressió; o poden ser immunoestimuladors, i activar la resposta immunitària inflamatòria contra el tumor, i frenar-ne el creixement. La proporció d’un tipus de macròfags o d’un altre determinarà si l’ambient que envolta el tumor n’afavoreix la progressió o si, per contra, activa el sistema immunitari contra les cèl·lules tumorals».
 En aquest treball, els investigadors han creuat les dades de més de 7.000 pacients de càncer de fins a 22 indicacions de tumor sòlid proporcionades pel projecte Altas del Genoma Humà del Càncer, amb els nivells de LIF que presentava el tumor i amb el tipus de macròfags associats al tumor ‒immunosupressors o immunoestimuladors.
En aquest treball, els investigadors han creuat les dades de més de 7.000 pacients de càncer de fins a 22 indicacions de tumor sòlid proporcionades pel projecte Altas del Genoma Humà del Càncer, amb els nivells de LIF que presentava el tumor i amb el tipus de macròfags associats al tumor ‒immunosupressors o immunoestimuladors.
«Els resultats d’aquestes anàlisis indiquen que, en pacients amb tumors que presenten nivells extremadament alts de LIF i macròfags immunosupressors, es pot predir que tindran una mala evolució de la malaltia. Aquestes dades suggereixen que LIF pot contribuir a la naturalesa immunosupressora dels macròfags i impulsar el creixement tumoral a través de la desactivació de la resposta immunitària», explica el Dr. Seoane.
El treball publicat a Clinical Cancer Research descriu com MSC-1 en inhibir LIF transforma els macròfags d’un estat immunosupressor protumoral a un estat immunoestimulador antitumoral i promou la infiltració de cèl·lules T al tumor. Això fa que hi hagi una resposta immunitària contra el tumor i un efecte antitumoral. «Hem observat que l´eficàcia d’MSC-1 es produeix, almenys en part, a través del canvi en les característiques dels macròfags i l´augment de la infiltració de cèl·lules immunes ‒cèl·lules T‒ per afavorir la immunitat antitumoral».
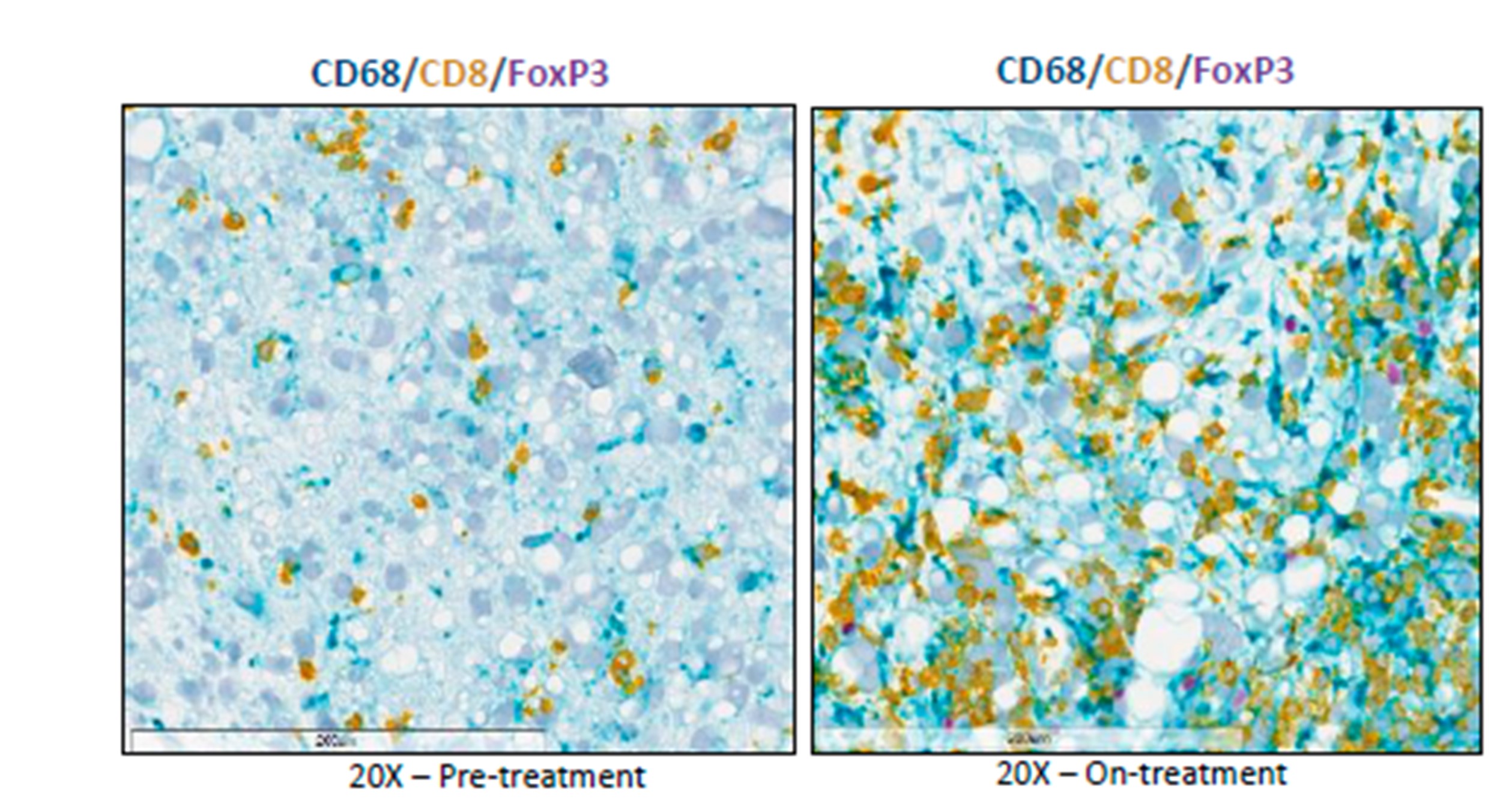
Aquestes dades es van poder validar a l’assaig clínic fase I a través de la caracterització de biòpsies abans i després del tractament. En aquestes mostres de pacients es va poder observar com el tractament canviava les característiques dels macròfags cap a macròfags immunoestimuladors i incrementava el nombre de cèl·lules immunes ‒cèl·lules T‒ al tumor. Aquestes observacions validaven en pacients els nostres resultats en models preclínics i implicaven que un tractament combinat amb MSC-1 i anti-PD-L1 podria ser efectiu. Aquest tractament s’està duent a terme a l’assaig fase II ja obert.
El Dr. Seoane va fundar Mosaic Biomedicals, una spin-off del VHIO nascuda per descobrir, desenvolupar i traslladar nous tractaments oncològics als pacients al més ràpid possible. Mosaic Biomedicals ha estat l’encarregada de portar un anticòs dirigit contra LIF ‒MSC-1‒, el primer de la seva categoria, a la clínica i fer un assaig fase I. L’assaig fase II d’MSC-1 ‒ara AZD0171‒ l’està duent a terme l’empresa Medimmune/AstraZeneca. Vall d’Hebron és un dels centres participants en l’assaig amb la Dra. Teresa Macarulla, cap del Grup de Tumors Gastrointestinals i Endocrins del VHIO i metgessa oncòloga de l’Hospital Universitari Vall d’Hebron, com a investigadora principal.
Tota la tasca preclínica i el desenvolupament dels assajos clínics per arribar a aprovar l’ús d’MSC-1 en pacients de càncer no serien possibles sense el finançament de de Loterías y Apuestas del Estado mitjançant l’Associació Espanyola Contra el Càncer, el Consell Europeu de Recerca, les fundacions Fero, Cellex, BBVA i la Fundació “la Caixa”.
Referències
Borazanci E, Schram AM, Garralda E, Brana I, Vieito Villar M, Spreafico A, Oliva M, Lakhani NJ, Hoffman K, Hallett RM, Maetzel D, Hua F, Hilbert J, Giblin P, Anido J, Kelly A, Vickers PJ, Wasserman R, Seoane J, Siu LL, Hyman DM, Hoff DV, Tabernero J. “Phase I, first-in-human study of MSC-1 (AZD0171), a humanized anti-leukemia inhibitory factor monoclonal antibody, for advanced solid tumors”. ESMO Open. 2022 Aug;7(4):100530. doi: 10.1016/j.esmoop.2022.100530. Epub 2022 Jul 31. PMID: 35921760; PMCID: PMC9434412.
Robin M. Hallett, Ester Bonfill-Teixidor, Raffaella Iurlaro, Alexandra Arias, Almudena Neva-Alejo, Swetha Raman, Peter Bayliss1, Olga Egorova, AJ Robert McGray, Esther Lau, Alexandre Bosch, Melissa Beilschmidt, Dorothea Maetzel, Johan Fransson, Isabel Huber-Ruano, Judit Anido, Jean-Philippe Julien, Patricia Giblin and Joan Seoane. “Therapeutic targeting of LIF overcomes macrophage mediated immunosuppression of the local tumor microenvironment”. Clin Cancer Res. 2022 Nov 28: CCR-21-1888. doi: 10.1158/1078-0432.CCR-21-1888. Epub ahead of print. PMID: 36441800.

















